体内细胞成像是理解驱动生物过程的时空动力学的重要工具。对于高度散射的组织,多光子显微术(MPM)的独特之处在于它能够深入完整的样本(200 um–2 mm,取决于组织)。由于激发光功率和荧光发射之间的非线性关系,散射激发光对检测到的荧光发射的贡献可忽略不计。因此,通过简单地增加入射激发功率,尽管大部分激发光散射离开焦点,局部荧光点仍可在样品深处成像。光漂白和光损伤的双重问题是每个荧光成像实验中不可避免的一部分。“光子预算”的概念通常用于表示样品健康、信号、空间分辨率和时间分辨率之间的内在权衡,一个广泛追求的目标是使显微镜在样品上尽可能柔和,同时仍然产生生物发现所需的对比度。这些问题在MPM是一个特别严重的问题。为了在散射组织中产生对比度,同时最小化光漂白和光毒性,它需要精确的、依赖于样本的激发功率随深度的增加。
近日,来自美国加州大学伯克利分校电气工程和计算机科学系、计算生物学研究生组的Henry Pinkard等人展示了自适应成像如何根据样本形状优化3D体积中每个点的照明功率,而不需要专门的荧光标记。他们的方法依赖于使用原位成像的具有相同荧光标记的细胞来训练基于物理的机器学习模型。他们使用这项技术对接种疫苗后小鼠淋巴结的免疫反应进行体内成像。他们实现了抗原特异性T细胞生理现实数量的可视化(比以前的研究低约2个数量级),并证明了在免疫反应的早期阶段树突细胞网络的整体组织和运动性的变化。他们为专门使用开源硬件和软件来实现这项技术提供了一个循序渐进的教程。相关研究工作发表在《Nature Communications》上。(詹若男)
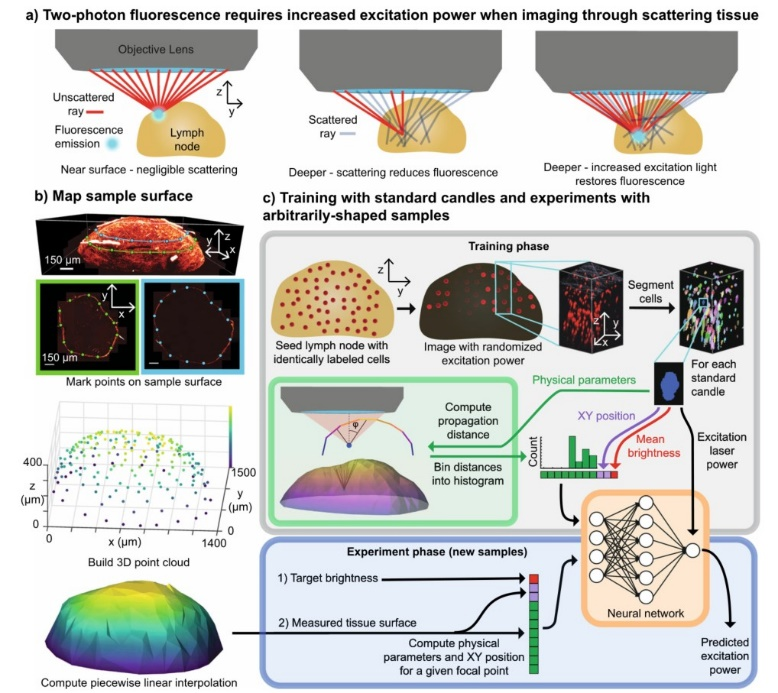
文章链接:Henry Pinkard et al. Learned adaptive multiphoton illumination microscopy for large-scale immune response imaging. Nature Communications (2021) 12:1916 https://doi.org/10.1038/s41467-021-22246-5
 客服热线:
客服热线: